Азотная кислота и её соли
Слайды и текст этой презентации
Это вещество является компонентом ракетного топлива, его использовали для двигателя первого в мире советского реактивного самолёта БИ – 1
Это вещество – прародитель большинства взрывчатых веществ (например, тротила, или тола)
— Это вещество в смеси с соляной кислотой растворяет платину и золото, признанное «царём» металлов. Сама смесь, состоящая из 1-ого объёма этого вещества и 3-ёх объёмов соляной кислоты, называется «царской водкой».
Азотная кислотаЯконюк Вера Сергеевна учитель химии МОУ Знаменская СОШ
Урок химии 9класс
Историческая справка
Строение
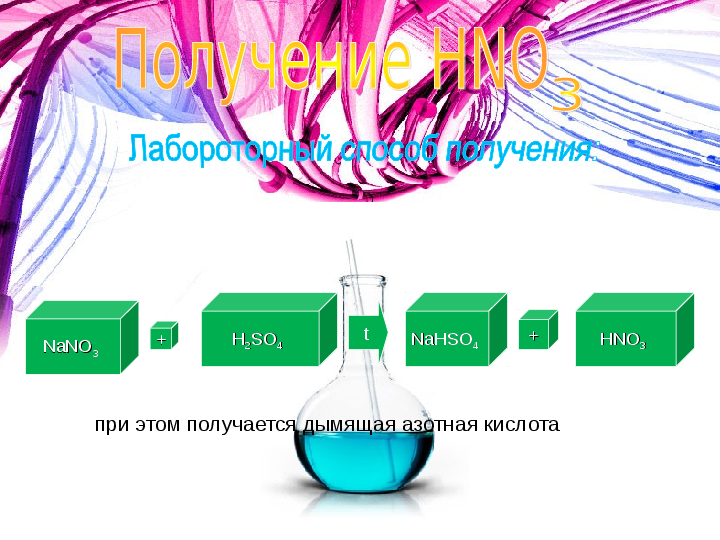
Получение.Лабороторный способ
Промышленный способ
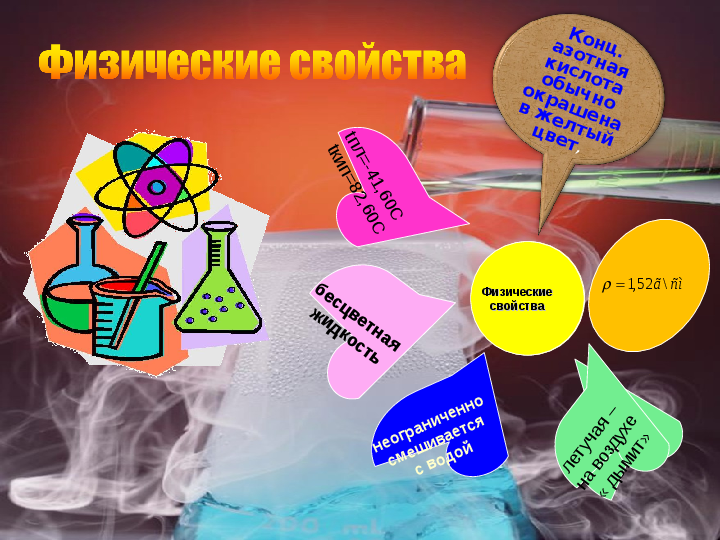
Физические свойства
Химические свойства.Общие с другими кислотами
Химические свойства.Специфические
Таблица
Применение
4KNO3 + 2(FeSO4 · 7H2O) (t°) → Fe2O3 + 2K2SO4 + 2HNO3↑ + NO2↑ + 13H2O
Чистую азотную кислоту получил впервые Иоганн Рудольф Глаубер, действуя на селитру концентрированной серной кислотой:KNO3 + H2SO4(конц.) (t°) → KHSO4 + HNO3↑
Дальнейшей дистилляцией может быть получена т. н. «дымящая азотная кислота», практически не содержащая воды
Историческая справка
Кристаллическая решетка – молекулярнаяСтроение
катализатора:
4NH3 + 5O2 = 4NO + 6H2O3. Поглощения NO2 водой в присутствии кислорода:
4NO2 + 2H2O + O2= 4HNO3
Массовая доля HNO3 составляет около 60%
2. Окисления NO в NO2 на холоду под давлением (10 ат):
2NO + O2 = 2NO2
свойствабесцветная
жидкость
tпл=-41,60C
tкип=82,60C
неограниченно
смешивается
с водой
летучая –
на воздухе
« дымит»
Конц. азотная кислота обычно окрашена в желтый цвет,
реакция ионного обмена, необратимая
CuO + 2H+ + 2 NO3- = Cu2+ + 2 NO3- + H2O
CuO + 2H+ = Cu2+ + H2O
Группа №2 CuCl2 + 2 NaOH = Cu(OH)2↓ + 2 NaCl
(получение нерастворимого основания)
Cu(OH)2 ↓+ 2 HNO3 = Cu(NO3)2 + 2 H2O —
реакция ионного обмена, необратимая
Cu(OH)2 ↓ + 2H+ + 2 NO3- = Cu2+ + 2 NO3- + 2 H2O
Cu(OH)2↓ + 2H+ = Cu2+ + 2 H2O
Признак реакции – растворение голубого осадка Cu(OH)2Группа №3 2 HNO3 + Na2CO3 = 2 NaNO3 + H2O + CO2 ↑ —
реакция ионного обмена, необратимая
2 H+ + 2NO3- + 2 Na+ + CO3 2- = 2 Na+ +NO3- + H2O + CO2↑
2 H+ + CO3 2- = H2O + CO2 ↑
Признак реакции – характерное «вскипание».
1) концентрация азотной кислоты;
2) активность металла
Комбинацией этих двух параметров и определяется состав продуктов реакции.
Что может быть?
а) металл может вступать в реакцию, а может не вступать (не реагировать вообще, пассивироваться);
б) состав газов смешанный (как правило выделяется не один газообразный продукт, а смесь газов, иногда какой-то газ преобладает над другими);
в) обычно водород в этих процессах не выделяется (есть исключение, когда на практике доказывается, что Mn + разб. HNO3 действительно выделяется газ водород)
Главное правило: Чем активнее металл и чем разбавленнее азотная кислота, тем глубже идёт восстановление азотной кислоты (крайний вариант — восстановление до амммиака NH3, точнее до NH4NO3 ; здесь процесс воссстановления N{+5} + 8e —-> N{-3} ). Возможны промежуточные варианты восстановления до NO2, NO, N2O, N2
Общая схема процесса:
HNO3 + Me —> соль азотной кислоты (нитрат) + продукт восстановления азотной кислоты + H2O
При взаимодействии с металлами образуются нитрат, вода и третий продукт по схеме:
HNO3(р.)+Me(до H2)→нитрат+H2O+NH3(NH4NO3)
HNO3(р.)+Me(после H2)→нитрат+H2O+NO
HNO3(к.)+Me(до H2)→нитрат+H2O+N2O(N2)
HNO3(к.)+Me(после H2)→нитрат+H2O+NO2
Концентрированная HNO3 на Al, Cr, Fe,Au, Pt не действует.
Li Na …….ZnМеталлы средней активности
Cr………..Sn
Металлы малоактивные и неактивные
Pb…………..Ag
Благородные металлы
Au Pt Os Ir
Конц
HNO3
Раз
HNO3
очень раз
HNO3
концHNO3
разHNO3
очень
Раз
HNO3
концHNO
разHNO3
Раств. только в царской водке-смеси 3об.HCl
B 1об. HNO3
NO
NO2
N2O или N2, NO2
NH3
(NHNO3)
Не реагируют
NO2,
,NO,N2O,NH3
NO2,
,NO,
N2O,
NH3
NO2
NO
P.S концентрированная HNO3 >60%
разбавленная HNO3 = 30-60%
очень разбавленная HNO3 < 30%
на холоде: железо, хром, алюминий пассивирует
Взаимодействие с металлами
-взрывчатых веществ (тринитротолуола и др.),
-органических красителей.
-как окислитель ракетного топлива.
— В металлургии Азотная кислота применяют для травления и растворения металлов, а также для разделения золота и серебра.
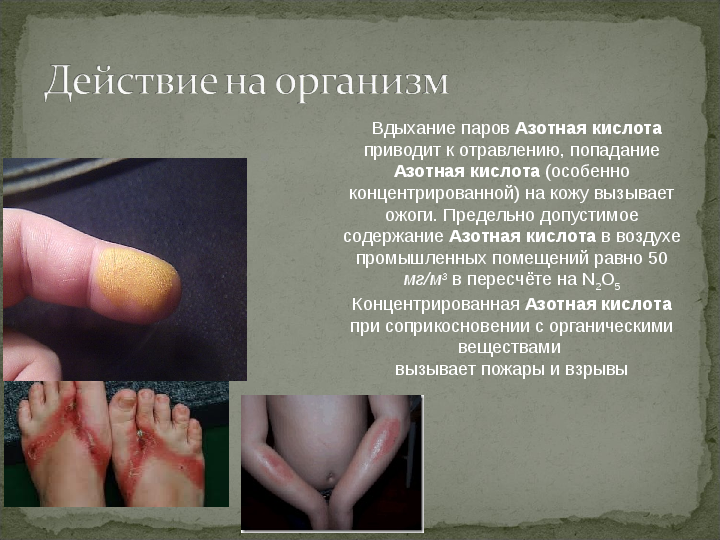
вызывает пожары и взрывы
При хранении на свету HNO3 а) краснеет б) желтеет в) остается бесцветной
При взаимодействии с металлами азотная кислота является: а)окислителем, б)восстановителем, в)и тем, и другим.
Азотная кислота в растворе не реагирует с веществом, формула которого:
а) CO2 ; б) NaOH; в) Al(OH)3 ; г) NH3 .
Царская водка- это а)концентрированный спирт б)3 объема HCl и 1 объем HNO3
в) концентрированная азотная кислота
реакция на индикатор, взаимодействие с оксидами металлов,
гидроксидами, солями более слабых кислот
обусловленные наличием в молекулах иона Н+;2. Сильные окислительные свойства азотной кислоты
обусловлены строением ее молекулы;
При ее взаимодействии с металлами
никогда не образуется водород,
а образуются нитраты, оксиды азота
или другие его соединения (азот, нитрат аммония)
и вода в зависимости от концентрации кислоты и активности металла;
3. Сильные окислительные способности HNO3
широко применяются для получения различных важных
продуктов народного хозяйства (удобрения, лекарства, пластики и т.д.)
Лидин Р.А., Молочко В.А., Андреева Л.Л. Химические свойства неорганических веществ Химия2000
http://ru.wikipedia.org/wiki/HNO3http://centralnyj.fis.ru/Petrochemicalshttp://dic.academic.ru/dic.nsf/bse/61981/%D0%90%D0%B7%D0%BE%D1