Галогены
Слайды и текст этой презентации
| Слайд №1 |
 |
Галогены(солеобразующие) |
| Слайд №2 |
 |
Общая характеристика галогенов
Галогены – это естественная группа элементов , расположенных в главной подгруппе 7 группы.
Фтор (F), хлор(Cl), бром (Br), йод (I), астат (At)
Галогены имеют степень окисления +1,+3,+5,+7, -1
У фтора только -1
В природе наиболее распространён- хлор. Астат получен искусственным путём. |
| Слайд №3 |
 |
+9
+53
+35
+17
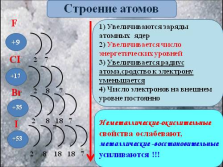
Неметаллические-окислительные свойства ослабевают,
металлические -восстановительные усиливаются !!!
2 7
2 8 7
2 8 18 7
2 8 18 18 7
F
CI
Br
I
1) Увеличиваются заряды атомных ядер
2) Увеличивается число энергетических уровней
3) Увеличивается радиус атома,сродство к электрону уменьшается
4) Число электронов на внешнем уровне постоянно
Строение атомов |
| Слайд №4 |
 |
F
1S22S22P5
S P
CI
1S22S22P63S23P5
Br
I
…4S24P5
…5S25P5
Электронные формулы
Вывод: галогены — р — элементы
На внешнем энергетическом
уровне 7 электронов, один из них неспаренный .
2
5 |
| Слайд №5 |
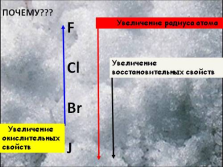 |
Увеличение восстановительных свойств
Увеличение окислительных свойств
Увеличение радиуса атома
F
Cl
Br
J
ПОЧЕМУ??? |
| Слайд №6 |
 |
-1
+7
-1
+3
-1
+5
-1
+1
0
Определите степени окисления атомов галогенов в веществах : |
| Слайд №7 |
 |
CI2
Br2
I2
F2
Простые
вещества
|
| Слайд №8 |
 |
:Г + Г: ? :Г(:) Г:
..
..
..
..
..
..
..
..
.
.
Химическая связь
К Н
Кристаллическая решетка
молекулярная
?
|
| Слайд №9 |
 |
Вещест
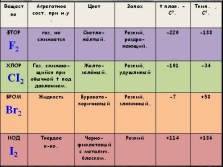
во Агрегатное сост. при н.у . Цвет Запах t плав. — C0. Tкип. , C0.
ФТОР
F2
газ, не сжижается Cветло- жёлтый. Резкий, раздра-жающий. -220 -188
ХЛОР
Газ, сжижаю-щийся при обычной t под давлением. Желто-зелёный. Резкий, удушливый -101 -34
БРОМ
Br2
Жидкость Буровато- коричневый Резкий, зловонный. -7 +58
ИОД
I2
Твердое
в-во. Черно-фиолетовый с металич. блеском. Резкий +114 +186
CI2 |
| Слайд №10 |
 |
1.Взаимодействие с металлами
Химические свойства галогенов
2 Na0 + CI20 = 2 NaCI
+1 -1
CI20 окислитель
Получаются соли: фториды,хлориды,бромиды,иодиды. |
| Слайд №11 |
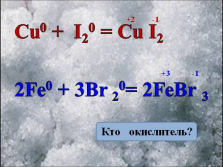 |
Cu0 + I20 = Cu I2
2Fe0 + 3Br 20= 2FeBr 3
+2 -1
+3 -1
Кто окислитель?
|
| Слайд №12 |
 |
2.Взаимодействие с водородом
Н20 + Г20 = 2Н Г
+1 -1
Н20 + CI20 = 2Н CI + Q
+1 -1
Н20 + F20 = 2Н F + Q
Н20 + Br20 = 2НBr
Н20 + I20 = 2Н I — Q
|
| Слайд №13 |
 |
3.Взаимодействие с водой
CI2 + H2O = HCI + HCIO
Хлорноватистая кислота
Соляная кислота
2F2 + 2Н2 О = 4НF + О2
плавиковая кислота |
| Слайд №14 |
 |
4.Взаимодействие с растворами солей
галогенов:
CI2
F2
Br2
I2
CI2 + 2NaBr = 2 NaBr + Br2
CI2 + 2NaI = 2 NaCl + I2
Br2 + 2NaI = 2 NaBr + I2
|
| Слайд №15 |
 |
Получение
В лаборатории*
МnO2 + 4HCI = MnCI2 + CI2 + 2H2O
+4 -1 +2 0
Mn+4 + 2e ? Mn+2 окислитель
восстанавливается
(О.В.)
2CI-1 – 2e ? CI20 восстановитель,
окисляется
(В.О.)
|
| Слайд №16 |
 |
В промышленности
Получают электролизом расплавов или растворов их солей.
2NaCl электролиз 2Na+Cl2
Расплав
|
| Слайд №17 |
 |
Дезинфицирующие реагенты
на основе хлора
Применение галогенов |
| Слайд №18 |
 |
Применение галогенов |
Оцените статью:
(1 голос, среднее: 4 из 5)
Поделитесь с друзьями!
Большой сборник презентаций в помощь школьнику.
закрыть
Скопируйте этот код и вставьте его на своем сайте:

