Щелочные металлы
Слайды и текст этой презентации
| Слайд №1 |
 |
9 класс
ЩЕЛОЧНЫЕ МЕТАЛЛЫ |
| Слайд №2 |
 |
Щелочные металлы |
| Слайд №3 |
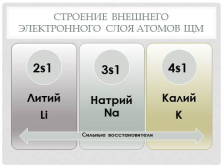 |
Строение внешнего электронного слоя атомов ЩМ
2s1
3s1
4s1
Сильные восстановители |
| Слайд №4 |
 |
Строение и свойства атомов
На внешнем энергетическом уровне все атомы содержат по одному электрону.
Атомы легко отдают электрон, поэтому являются очень сильными восстановителями.
|
| Слайд №5 |
 |
Характеристика атомов |
| Слайд №6 |
 |
Щелочные металлы — простые вещества |
| Слайд №7 |
 |
Химические свойства ЩМ |
| Слайд №8 |
 |
|
| Слайд №9 |
 |
Реакция с водой
ЩМ активно реагируют с водой, образуя щелочи и водород.
2Na + 2Н2О = 2NaОН + H2
Скорость реакции ЩМ с водой увеличивается от Li к Cs. |
| Слайд №10 |
 |
Реакция с кислородом |
Оцените статью:
(0 голосов, среднее: 0 из 5)
Поделитесь с друзьями!
Большой сборник презентаций в помощь школьнику.
закрыть
Скопируйте этот код и вставьте его на своем сайте:

