Водород — химический элемент и простое вещество
Слайды и текст этой презентации
| Слайд №1 |
 |
Водород – химический элемент и простое вещество
Эпитеты: наипервейший, вездесущий, всемогущий и невидимый
Анаграмма
Первый слог вещества, которое имеет три агрегатных состояния.Второй слог – первая нота.Третий слог – указывает родство.
Тема урока?
Генри Кавендиш |
| Слайд №2 |
 |
Девиз урока:
Всегда держись начеку
(Козьма Прутков) |
| Слайд №3 |
 |
Составление плана работыПосмотрите структуру параграфа № 17 (с.98-103) и дополните план изучения водорода:
1. Водород – химический элемент: а) положение в ПСХЭ Д.И. Менделеева,
б) строение атома. 2. Водород – простое вещество: а) строение молекулы, б) физические свойства, в) химические свойства, г) получение и применение и водорода |
| Слайд №4 |
 |
Положение водорода в ПСХЭ Д. И. Менделеева
Чтобы определить положение водорода в ПСХЭ, воспользуемся динамической таблицей периодической системы элементов, расположенной по электронному адресу:
Ссылка № 1 Открытая техническая библиотека CNCexpert.ru (воспользуемся динамической таблицей периодической системы элементов)
http://cncexpert.ru/chemistry/periodic-table.php
|
| Слайд №5 |
 |
Вывод: водород- единственный элемент, для которого химики отводят в периодической системе 2 места – да каких! Его записывают в 2 резко противоположные группы химических элементов:
— в главной подгруппе 1 группы – подгруппе щелочные металлы
в главной подгруппе 7 группы- подгруппе галогены.
Возникает вопрос. Почему?
Прежде чем сформулировать ответ, посмотрите фрагмент «Модель атома водорода». Для этого перейдите по
ссылке № 2 ЦОРы http://school-collection.edu.ru/catalog/search/?text=%E2%EE%E4%EE%F0%EE%E4&tg=
В строке найти введите водород, откройте документ № 7 «Модель атома водорода»
При затруднении ответить, обратитесь дополнительно к учебнику стр.98 |
| Слайд №6 |
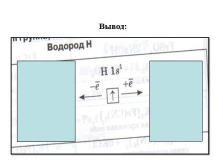 |
Вывод: |
| Слайд №7 |
 |
Строение молекулы водорода
Пользуясь информацией из интернет-энциклопедии Википедия (ссылка № 3) опишите строение молекулы водорода и сделайте в тетради её рисунок
Вывод: молекула двухатомна, образована за счет ковалентной неполярной химической связи. |
| Слайд №8 |
 |
Агрегатное состояние газ
Цвет бесцветный
Запах нет
Растворимость в воде малорастворим
Молекулярная масса (по сравнению с воздухом) 2 (29-воздух)
Во сколько раз легче воздуха 14
Закрепление:
Посмотрев видеофрагменты Единой коллекции ЦОРов
ссылка № 4, 5 (нерастворимость водорода в воде, «Мыльные пузыри с водородом») выделите в таблице те физические свойства водорода, которым посвящены видеофрагменты.
Закрепление:
Посмотрев видеофрагменты Единой коллекции ЦОРов
ссылка № 4, 5 (нерастворимость водорода в воде, «Мыльные пузыри с водородом») выделите в таблице те физические свойства водорода, которым посвящены видеофрагменты.
Физические свойства водорода
Возвращаясь к динамической таблицей периодической системы элементов (к ссылке № 1)
http://cncexpert.ru/technical-glossary/hydrogen.php)
заполните правую колонку таблицы (информация из таблицы – элемент Н, работа по активным ссылкам)
«Физические свойства водорода» |
| Слайд №9 |
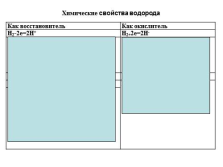 |
Химические свойства водорода
Как восстановитель Как окислитель
H2-2e=2H+ H2+2e=2H-
2H2 + O2 = 2H2O
ссылка № 6 http://school-collection.iv-edu.ru/dlrstore/36fbfc5d-cb25-31b9-808b-36c1e8086a0a/index.htm H2 + 2Na = 2NaH
3H2 + N2 = 2NH3 H2 + Ca = CaH2
H2 + Cl2 = 2HCl В результате образуются гидриды-твердые, солеподобные соединения
CuO + H2 = Cu + H2O
ссылка № 7
Сhttp://files.school-collection.edu.ru/dlrstore/6350fa30-2229-9816-a557-cfd1f53489ed/index.htm В результате образуются гидриды-твердые, солеподобные соединения |
| Слайд №10 |
 |
Получение водорода
В лаборатории
Прочитав инструкцию и посмотрев видеоопыт
ссылка № 8 «Получение, собирание, распознавание водорода», проведите самостоятельно этот лабораторный опыт (соблюдая ТБ!), запишите уравнение реакции, где расставите коэффициенты методом электронного баланса и выявите, чем будет являться водород окислителем или восстановителем
Zn + 2HCl = ZnCl2 + H2? |
| Слайд №11 |
 |
В промышленности
Задание по группам:
каждой группе необходимо дописать уравнение реакции получения водорода, где расставить коэффициенты методом электронного баланса и выявить, чем будет являться водород окислителем или восстановителем, когда вы это сделаете один учащийся от группы выйдет и закончит УХР на доске
1.Электролиз водных растворов солей:
2NaCl + 2H2O ? H2 + 2NaOH + Cl2
2.Пропускание паров воды над раскаленным коксом при температуре около 1000°C:
H2O + C ? H2 + CO
3.Из природного газа.
Конверсия с водяным паром:
CH4 + H2O ? CO + 3H2 (1000°C)
Каталитическое окисление кислородом:
2CH4 + O2 ? 2CO + 4H2 |
| Слайд №12 |
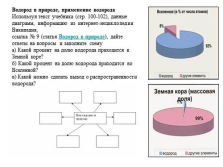 |
Водород в природе, применение водорода
Используя текст учебника (стр. 100-102), данные диаграмм, информацию из интернет-энциклопедии Википедия,
ссылка № 9 (статья Водород в природе), дайте ответы на вопросы и заполните схему
а) Какой процент на долю водорода приходится в Земной коре?
б) Какой процент на долю водорода приходится во Вселенной?
в) Какой можно сделать вывод о распространенности водорода?
|
| Слайд №13 |
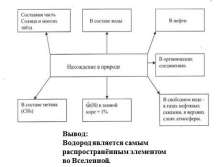 |
Вывод:
Водород является самым распространённым элементом во Вселенной. |
| Слайд №14 |
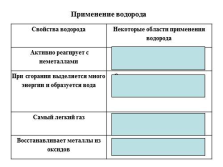 |
Применение водорода
Свойства водорода Некоторые области применения водорода
Активно реагирует с неметаллами Производство аммиака, соляной кислоты, органических веществ
При сгорании выделяется много энергии и образуется вода Энергетическая промышленность
Самый легкий газ Наполнение воздушных шаров и аэростатотов
Восстанавливает металлы из оксидов Получение металлов |
| Слайд №15 |
 |
Прочитав информацию на слайде презентации ответьте на вопрос:
Какое свойство водорода делает его опасным для наполнения аэростатов?
Если шар объёмом 22,4 м3 наполнить водородом, то в воздухе он может поднять груз массой 27 кг. В первой половине XX века началось строительство летательных аппаратов большой грузоподъёмности — дирижаблей, которые наполняли водородом. Однако водород — взрывоопасный газ, и в 1930-е гг. с дирижаблями произошло несколько крупных аварий. После этого строительство дирижаблей с водородом во всём мире на многие годы прекратилось. |
| Слайд №16 |
 |
Закрепление
Ссылка № 9 Федеральный центр информационно-образовательных ресурсов
Тест по теме «Водород»
Время выполнения 3 минуты
|
| Слайд №17 |
 |
Лист самоанализа усвоения нового материала
Вопрос «5» «4» «3» «2»
Место Н в ПСХЭ
Строение атома и молекулы
Нахождение в природе, применение
Физические свойства
Химические свойства
Получение
§17, зад. 3, 4 стр.103
Домашнее задание |
Оцените статью:
(1 голос, среднее: 3 из 5)
Поделитесь с друзьями!
Большой сборник презентаций в помощь школьнику.
закрыть
Скопируйте этот код и вставьте его на своем сайте: