Кислоты
Слайды и текст этой презентации
| Слайд №1 |
 |
Распределите эти формулы по классам в таблицу
оксиды основания
HCl, HNO3, H2SO4, Ca(OH)2, K2O, Na2O, Al2O3, Zn(OH)2, Fe(OH)3
ответ |
| Слайд №2 |
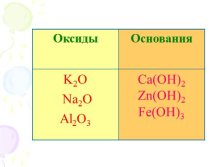 |
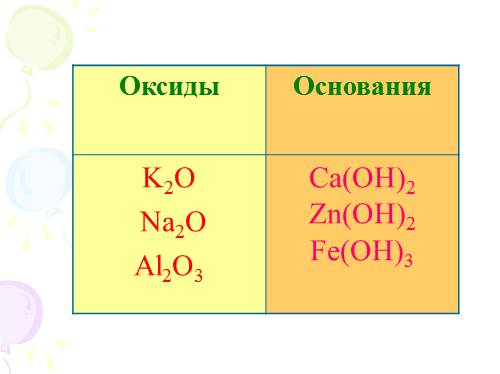
Оксиды Основания
K2O
Na2O
Al2O3 Ca(OH)2 Zn(OH)2 Fe(OH)3
|
| Слайд №3 |
 |
Тема: Кислоты |
| Слайд №4 |
 |
ОРГАНИЧЕСКИЕ –
ЛИМОННАЯ, ЯБЛОЧНАЯ, УКСУСНАЯ, ЩАВЕЛЕВАЯ, МУРАВЬИНАЯ.
По происхождению кислоты бывают |
| Слайд №5 |
 |
НЕОРГАНИЧЕСКИЕ-
СЕРНАЯ, СОЛЯНАЯ, ПЛАВИКОВАЯ, ФОСФОРНАЯ, АЗОТНАЯ. |
| Слайд №6 |
 |
Соляная кислота, находящаяся в желудке, помогает переваривать пищу.
Молочная кислота
образуется в мышцах при физической нагрузке.
КИСЛОТЫ СОДЕРЖАТСЯ В ОРГАНИЗМАХ ЖИВОТНЫХ |
| Слайд №7 |
 |
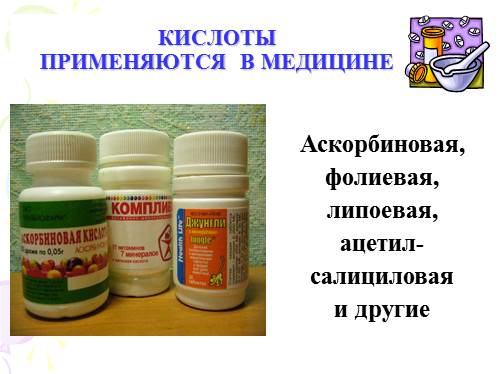
КИСЛОТЫ ПРИМЕНЯЮТСЯ В МЕДИЦИНЕ
Аскорбиновая,
фолиевая,
липоевая,
ацетил-
салициловая
и другие |
| Слайд №8 |
 |
КИСЛОТЫ ПРИМЕНЯЮТСЯ В КУЛИНАРИИ
Уксусная и
лимонная кислоты |
| Слайд №9 |
 |
ДЕЙСТВИЕ КИСЛОТ НА ИНДИКАТОРЫ
Индикатор Окраска индикатора в растворе соляной кислоты (HCl)
Индикаторная бумага красная
Фенолфталеин бесцветный
Метилоранж Красно-розовый |
| Слайд №10 |
 |
Прочитайте формулы кислот. HCl, H2SO4, H3PO4
Кислоты – это сложные вещества, состоящие из ионов водорода и кислотного остатка.
Что общего во всех этих формулах?
все общие свойства кислот,
в том числе изменение окраски индикаторов,
связаны с элементом водородом.
Остальная часть молекулы называется кислотным остатком. |
| Слайд №11 |
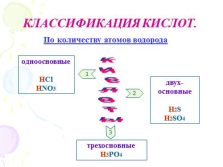 |
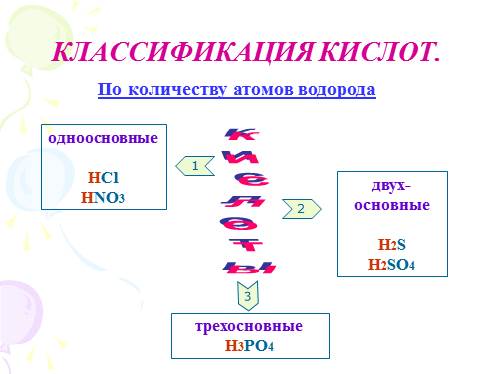
КЛАССИФИКАЦИЯ КИСЛОТ.
кислоты
2
1
3
одноосновные
HCl
HNO3
двух-
основные
H2S
H2SO4
трехосновные
H3PO4
По количеству атомов водорода |
| Слайд №12 |
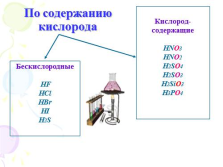 |
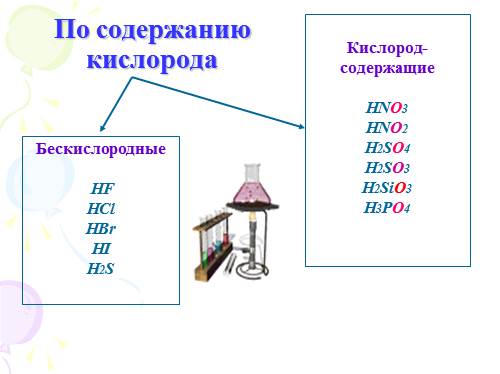
По содержанию кислорода
Бескислородные
HF
HCl
HBr
HI
H2S
Кислород-
содержащие
HNO3
HNO2
H2SO4
H2SO3
H2SiO3
H3PO4
|
| Слайд №13 |
 |
Формула Название
HF плавиковая
HCL соляная
HBr Бромоводородная
HI Йодоводородная
H2S Сероводородная |
| Слайд №14 |
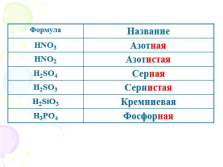 |
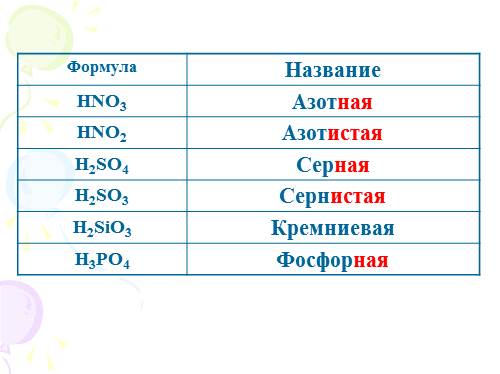
Формула Название
HNO3 Азотная
HNO2 Азотистая
H2SO4 Серная
H2SO3 Сернистая
H2SiO3 Кремниевая
H3PO4 Фосфорная |
| Слайд №15 |
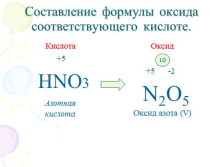 |
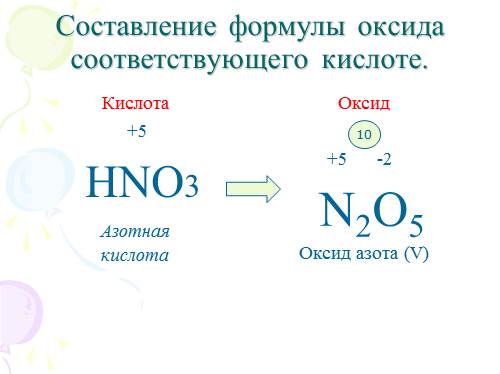
Составление формулы оксида соответствующего кислоте.
Кислота
+5
HNO3
Азотная
кислота
Оксид
+5 -2
N O
Оксид азота (V)
10
N2O5 |
| Слайд №16 |
 |
Серная кислота Н2SO4
Бесцветная жидкость, вязкая как масло, не имеющая запаха. В 2 раза тяжелее воды. |
| Слайд №17 |
 |
Техника безопасности
При растворении серной кислоты нужно вливать её тонкой струёй в воду при помешивании |
| Слайд №18 |
 |
Домашнее задание:
§ 20, учить формулы и названия кислот,
подготовиться к химическому диктанту |
Оцените статью:
(7 голосов, среднее: 5 из 5)
Поделитесь с друзьями!
Большой сборник презентаций в помощь школьнику.
закрыть
Скопируйте этот код и вставьте его на своем сайте: